陽明大學與台北榮總頭頸癌研究團隊20日發表重大研究成果,發現晚期頭頸癌的腫瘤細胞組織,若呈現兩個壞的蛋白被活化、好的RNA被抑制,會使得局部高侵襲性的訊號被開啟,解答臨床上患者預後不佳的原因,也替未來新藥發展找出明確的分子標記,此成果本月獲刊於國際權威期刊。
發表研究的是陽明大學臨床醫學研究所副教授、台北榮總血液腫瘤科醫師楊慕華,他指出不同於其他腫瘤晚期多遠端轉移,晚期頭頸癌的特徵是局部高侵襲性,造成頭頸組織壓迫,最常造成患者吞嚥與發聲困難,目前治療困境是手術會導致患者外觀巨大改變,且對化療、放療的治療效果不彰。
楊慕華醫師的團隊找出了晚期頭頸癌具局部高侵襲性的成因,源自有一個轉移蛋白Twist1被啟動,打開了局部侵襲訊號的開關,導致好的RNA let-7i被抑制、壞的蛋白RAC1被活化,研究發現有這些分子標記的患者,預後較差,此研究獲刊國際權威期刊「自然細胞生物學」。
楊慕華醫師指出,也由於這三個分子表現缺一不可,因此若能透過藥理改變其中一環,就能破壞局部侵襲的訊息傳導,透過動物以及細胞實驗發現,抑制RAC1蛋白的可行性最高,也成為未來新藥發展的分子標的,可作為未來專一治療方向。
這項侵襲訊息傳導的分子診斷,可輔助現有的病理切片診斷,可更明確找出未來可能有局部高侵襲性的頭頸癌患者,楊慕華醫師指出,對這些預後較差的患者,在新藥發展出來之前,建議在治療上提高劑量或延長使用時間,以更有效控制腫瘤。


 頭頸癌不怕!引導性化學治療新選擇
頭頸癌不怕!引導性化學治療新選擇
 漫談頭頸部癌及食道癌
漫談頭頸部癌及食道癌
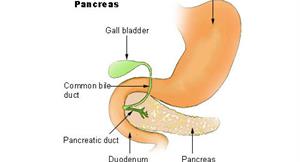 成大組跨國胰臟癌團隊 擬研發新藥救命
成大組跨國胰臟癌團隊 擬研發新藥救命
 童綜合白沙屯媽祖醫院開工動土典禮!預計118年竣工落成啟用
童綜合白沙屯媽祖醫院開工動土典禮!預計118年竣工落成啟用
 《子宮頸癌小學堂》:從HPV、抹片檢查到癌前病變,陪妳一步步安心了解
《子宮頸癌小學堂》:從HPV、抹片檢查到癌前病變,陪妳一步步安心了解
 研究:3成年輕運動員猝死主因竟是它!肥厚型心肌病變治療邁入精準新時代
研究:3成年輕運動員猝死主因竟是它!肥厚型心肌病變治療邁入精準新時代








 闽公网安备 35020302001899号
闽公网安备 35020302001899号
